In der Natur kommt Aluminiumsulfat in Form des Minerals Alunogen vor. Weiterhin kann es aus natürlich vorkommenden Alaunen gewonnen werden.
Aluminiumsulfat
Aluminiumsulfat, Summenformel Al2(SO4)3, ist eine chemische Verbindung des Aluminiums aus der Gruppe der Sulfate. Es bildet ein farbloses Pulver mit einer Dichte von 2,71 g/cm3.

Das Hydrat des Aluminiumsulfats lässt sich durch Auflösen von reinem Aluminiumoxid oder Aluminiumhydroxid in konzentrierter Schwefelsäure gewinnen.
Im Bereich von Lebensmittelzusatzstoffe agieren zahlreiche Unternehmen, die mit ihren Produkten und Dienstleistungen Lösungen für dieses Thema anbieten. Die Firmenliste bietet einen umfassenden Überblick über die Akteure, die im Bereich Lebensmittelzusatzstoffe eine Schlüsselrolle spielen. Von etablierten Branchenführern bis hin zu aufstrebenden Start-ups, jedes Unternehmen trägt auf seine Weise zur Dynamik und Entwicklung von Lebensmittelzusatzstoffe bei.
| Unternehmen | Herkunft | Typ |
|---|---|---|

|
Laudenbach, Deutschland | Hersteller |

|
Burnaby, Kanada | Hersteller |
|
|
Stetten SH, Schweiz | Hersteller |

|
Hamburg, Deutschland | Hersteller |

|
Zürich, Schweiz | Dienstleister |

|
Marly, Schweiz | Hersteller |

|
Emmerthal, Deutschland | Hersteller |

|
Lausanne, Schweiz | Dienstleister |
|
|
Düsseldorf, Deutschland | Händler |

|
Hamburg, Deutschland | Hersteller |
Mit saurer Reaktion löst sich Aluminiumsulfat in Wasser und kristallisiert bei Zimmertemperatur als monoklines Al2(SO4)3 · 18 H2O aus. Ab einer Temperatur von 340 °C findet eine vollständige Dehydratisierung des Salzes statt und oberhalb von 770 °C zerfällt es in Aluminiumoxid und Schwefeltrioxid.
Aluminiumsulfat bildet mit den Sulfaten einwertiger Metalle Doppelsalze gemäß folgender Formel (Alaune):
Aluminiumsulfat findet folgende Verwendungen:
- Retentionsmittel und zur Leimung in der Papierherstellung
- Flockungsmittel in der Trinkwasseraufbereitung und Abwasseraufbereitung
- Beizmittel in der Färberei
- Saatgutbeize
- Bestandteil von Schaumlöschmitteln
- Flammschutzmittel
- Isoliersalz (auf frischen Zement- oder Kalkuntergründen, gegen Wasser- und Nikotinflecken) in der Renovierung
- Inhaltsstoff von Pflanzenstärkungs- und schutzmitteln und zur Blaufärbung von Hortensien
- Festigungsmittel bzw. Stabilisator in Lebensmitteln, in der EU als Lebensmittelzusatzstoff E 520 zugelassen.
In der Welt des Themas Lebensmittelzusatzstoffe gibt es ständig Neues zu entdecken. Aktuelle Entwicklungen und spannende Meldungen bieten tiefe Einblicke und erweitern das Verständnis für dieses dynamische Feld. Von bahnbrechenden Entdeckungen bis hin zu wichtigen Ereignissen – die Entwicklungen für das Thema Lebensmittelzusatzstoffe sind ein Spiegelbild des stetigen Wandels und der Innovation in diesem Bereich.
Bei einem Vorfall mit Aluminiumsulfat im Trinkwasser in Camelford in Cornwall in England trank im Juli 1988 eine Reihe von Menschen Trinkwasser mit größeren Konzentrationen an Aluminiumsulfat. Die zulässigen Grenzwerte waren um das 5000-fache überschritten. Nach dem Unfall klagten zahlreiche Anwohner unter anderem über Geschwüre, Hautausschlag und Gedächtnisprobleme. Ein Todesfall im Jahr 2006 hat eine Debatte über Spätfolgen des Unglücks intensiviert. Die Untersuchungen der langfristigen Auswirkungen auf die Gesundheit nach diesem Vorfall sind noch immer nicht vollständig abgeschlossen, aber es wurden in Post-Mortem-Untersuchungen besonders stark erhöhte Aluminium-Konzentrationen in den Gehirnen der Opfer festgestellt und weitere Untersuchungen in Auftrag gegeben, um festzustellen, ob es einen Zusammenhang mit Zerebraler Amyloidangiopathie gibt.
Aluminiumsulfat wurde 2013 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Aluminiumsulfat waren die Besorgnisse bezüglich Verbraucherverwendung, hoher (aggregierter) Tonnage, hohes Risikoverhältnis (Risk Characterisation Ratio, RCR) und weit verbreiteter Verwendung sowie der Gefahren ausgehend von einer möglichen Zuordnung zur Gruppe der CMR-Substanzen und der möglichen Gefahr durch sensibilisierende Eigenschaften. Die Neubewertung fand ab 2015 statt und wurde von Frankreich durchgeführt.
Im Bereich von Lebensmittelzusatzstoffe bieten White Papers und Fachartikel weitergehende Einblicke und fundiertes Wissen. Diese Sammlung von Fachwissen bietet Ressourcen für alle, die sich eingehend mit den Facetten und Nuancen des Themas Lebensmittelzusatzstoffe beschäftigen möchten. Diese Auswahl an Veröffentlichungen deckt ein breites Spektrum ab – von theoretischen Überlegungen bis hin zu praktischen Anwendungen und Fallstudien - und umfasst Arbeiten von Experten, die Licht auf die komplexen Aspekte von Lebensmittelzusatzstoffe werfen.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 ![{mathrm { ! {Biggr ]}_{2}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/574adab1409cb81da6c38bb738ad111e61bbb2d9)  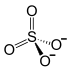 ![{mathrm { ! {Biggr ]}_{3}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/cd32744e9f4314d390f5ee107a8bd812d0cc2da0) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Aluminiumsulfat | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | Al2(SO4)3 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose Kristalle | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 342,13 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
2,71 g·cm−3 | |||||||||||||||||||||
| Schmelzpunkt |
770 °C (Zersetzung) | |||||||||||||||||||||
| Löslichkeit |
leicht in Wasser (360 g·l−1 bei 20 °C) | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
6 mg·m−3 (Al) | |||||||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||||||||
| ΔHf0 |
−3442 kJ·mol−1 | |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||

Holen Sie sich die Lebensmittel- und Getränke-Branche in Ihren Posteingang
Ab sofort nichts mehr verpassen: Unser Newsletter für die Lebensmittel- und Getränkeindustrie bringt Sie jeden Dienstag und Donnerstag auf den neuesten Stand. Aktuelle Branchen-News, Produkt-Highlights und Innovationen - kompakt und verständlich in Ihrem Posteingang. Von uns recherchiert, damit Sie es nicht tun müssen.








